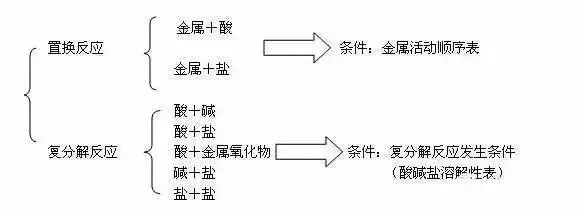
ę╗��Īó╦ßĪóēA�Īó¹}Ą─ĮM│╔
╦ß╩Ūė╔Üõį¬╦ž║═╦ßĖ∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║┴“╦ß(H2SO4)�����Īó¹}╦ß(HCl)���ĪóŽ§╦ß(HNO3)
ēA╩Ūė╔Įī┘į¬╦ž║═Üõč§Ė∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║Üõč§╗»Ōc����ĪóÜõč§╗»Ō}���Īó░▒╦«(NH3·H2O)
¹}╩Ūė╔Įī┘į¬╦žį¬╦ž(╗“õ@Ė∙)║═╦ßĖ∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║┬╚╗»Ōc����Īó╠╝╦ßŌc
╦ßĪóēA��Īó¹}Ą─╦«╚▄ę║┐╔ęįī¦(d©Żo)ļŖ(įŁę“Ż║╚▄ė┌╦«ĢrļxĮŌą╬│╔ūįė╔ęŲäėĄ─ĻÄ��ĪóĻ¢ļxūė)
Č■��Īó╦ß
1�����ĪóØŌ¹}╦ß����ĪóØŌ┴“╦ߥ─╬’└Ēąį┘|(zh©¼)Īó╠žąį���Īóė├═Š
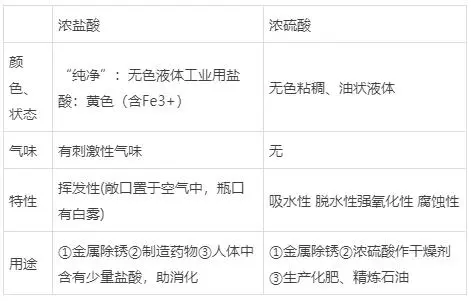
2�����Īó╦ߥ─═©ąį(Š▀ėą═©ąįĄ─įŁę“Ż║╦ßļxĮŌĢr╦∙╔·│╔Ą─Ļ¢ļxūė╚½▓┐╩ŪH+)
(1)┼c╦ßēAųĖ╩Šä®Ą─Ę┤æ¬(y©®ng)Ż║╩╣ūŽ╔½╩»╚’įćę║ūā╝t╔½Ż¼▓╗─▄╩╣¤o╔½Ęė╠¬įćę║ūā╔½
(2)Įī┘ + ╦ß → ¹} + ÜõÜŌ
(3)ēAąįč§╗»╬’ + ╦ß → ¹} + ╦«
(4)ēA + ╦ß → ¹} + ╦«
(5)¹} + ╦ß → ┴Ēę╗ĘN¹} + ┴Ēę╗ĘN╦ß(«a(ch©Żn)╬’Ę¹║ŽÅ═(f©┤)ĘųĮŌŚl╝■)
3����Īó╚²ĘNļxūėĄ─Öz“×(y©żn)

╚²����ĪóēA
1�ĪóÜõč§╗»ŌcĪóÜõč§╗»Ō}Ą─╬’└Ēąį┘|(zh©¼)����Īóė├═Š
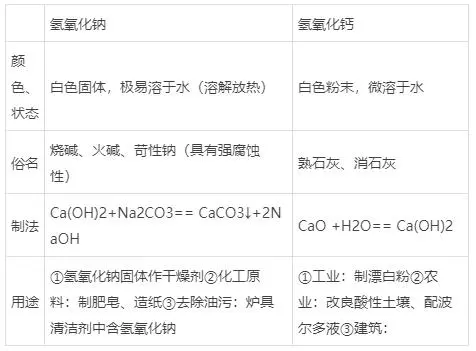
2ĪóēAĄ─═©ąį(Š▀ėą═©ąįĄ─įŁę“Ż║ļxĮŌĢr╦∙╔·│╔Ą─ĻÄļxūė╚½▓┐╩ŪOH-)
(1)ēA╚▄ę║┼c╦ßēAųĖ╩Šä®Ą─Ę┤æ¬(y©®ng)Ż║╩╣ūŽ╔½╩»╚’įćę║ūā╦{(l©ón)╔½����Ż¼╩╣¤o╔½Ęė╠¬įćę║ūā╝t╔½
(2)╦ßąįč§╗»╬’+ēA → ¹}+╦«
(3)╦ß+ēA → ¹}+╦«
(4)¹}+ēA → ┴Ēę╗ĘN¹}+┴Ēę╗ĘNēA(Ę┤æ¬(y©®ng)╬’Š∙┐╔╚▄Ż¼«a(ch©Żn)╬’Ę¹║ŽÅ═(f©┤)ĘųĮŌŚl╝■)
ūóŻ║ó┘ļy╚▄ąįēA╩▄¤ßęūĘųĮŌ(▓╗ī┘ė┌ēAĄ─═©ąį)
╚ńCu(OH)2 ΔCuO +H2O
2Fe(OH)3 ΔFe2O3+3H2O
ó┌│ŻęŖ│┴ĄĒŻ║AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓
ó█Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)Ą─Śl╝■Ż║«ö(d©Īng)ā╔ĘN╗»║Ž╬’╗źŽÓĮ╗ōQ│╔Ęų�Ż¼╔·│╔╬’ųąėą│┴ĄĒ╗“ėąÜŌ¾w╗“ėą╦«╔·│╔ĢrŻ¼Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)▓┼┐╔ęį░l(f©Ī)╔·�ĪŻ
╦─Īó╦ßąįč§╗»╬’┼cēAąįč§╗»╬’
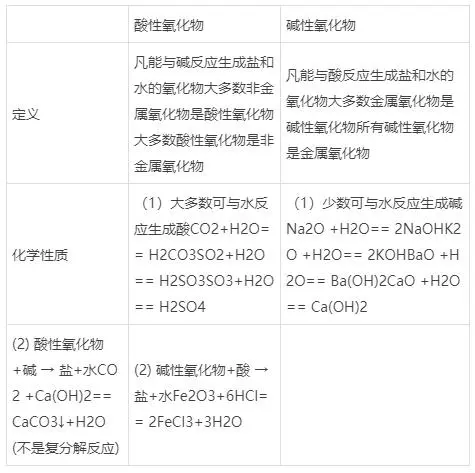
╬Õ���Īóųą║═Ę┤æ¬(y©®ng) ╚▄ę║╦ßēAČ╚Ą─▒Ē╩ŠĘ©--pH
1��ĪóČ©┴xŻ║╦ß┼cēAū„ė├╔·│╔¹}║═╦«Ą─Ę┤æ¬(y©®ng)
2�����Īóæ¬(y©®ng)ė├Ż║
(1)Ė─ūā═┴╚└Ą─╦ßēAąį
(2)╠Ä└Ē╣żÅSĄ─ÅU╦«
(3)ė├ė┌ßt(y©®)╦Ä
3�����Īó╚▄ę║╦ßēAČ╚Ą─▒Ē╩ŠĘ©--pH
(1)pHĄ─£yČ©Ż║ūŅ║åå╬Ą─ĘĮĘ©╩Ū╩╣ė├pHįć╝ł
ė├▓Ż┴¦░¶(╗“Ą╬╣▄)š║╚Ī┤²£yįćę║╔┘įS��Ż¼Ą╬į┌pHįć╝ł╔Ž��Ż¼’@╔½║¾┼cś╦(bi©Īo)£╩(zh©│n)▒╚╔½┐©ī”šš�Ż¼ūx│÷╚▄ę║Ą─pH(ūxöĄ(sh©┤)×ķš¹öĄ(sh©┤))
(2)╦ßėĻŻ║š²│ŻėĻ╦«Ą─pH╝s×ķ5.6(ę“?y©żn)ķ╚▄ėąCO2)
pH<5.6Ą─ėĻ╦«×ķ╦ßėĻ
╦ßēA¹}ąį┘|(zh©¼)ų«╦ߥ─═©ąį
╦ߥ─ĮM│╔——Üõļxūė+╦ßĖ∙ļxūė
(1)Ė·ųĖ╩Šä®Ę┤æ¬(y©®ng)
ūŽ╔½╩»╚’įćę║ė÷╦ßūā╝t╔½
¤o╔½Ęė╠¬įćę║ė÷╦ß▓╗ūā╔½
(2)╦ߥ─PH<7
(3)Ė·(H)Ū░Ą─╗ŅØŖĮī┘Ųų├ōQĘ┤æ¬(y©®ng)
╦ß + Įī┘==¹} + ÜõÜŌ
└²Ż║2HCl+Fe=FeCl2+H2↑
(4) Ė·ēAąįč§╗»╬’║═─│ą®Įī┘č§╗»╬’Ę┤æ¬(y©®ng)
╦ß + ēAąį(Įī┘)č§╗»╬’—→¹}+╦«
└²Ż║3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
(5)Ė·─│ą®¹}Ę┤æ¬(y©®ng)
╦ß+╠╝╦ß¹}==¹}+╦«
╦ß+¹}—→ą┬╦ß+ą┬¹}
└²Ż║H2SO4+BaCl2=2HCl+BaSO4↓
(6)Ė·ēAŲųą║═Ę┤æ¬(y©®ng)
╦ß+ēA—→¹}+╦«
└²Ż║2HCl+Cu(OH)2=CuCl2+2H2O
│§ųą╗»īW(xu©”)╦ßēA¹}Ą─Å═(f©┤)┴Ģ(x©¬)╝░ųž³c(di©Żn)Ņ}ą═ĮŌ╬÷
į┌Ė„╩Ī╩ąųą┐╝įćŠĒĄ─├³Ņ}ųąŻ¼¤o▓╗īó╦ßēA¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)Ą─┐╝▓ņū„×ķųžųąų«ųž���ĪŻŲõŅ}ą═ų«ČÓūā╗»ų«┤¾����Ż¼ī”ė┌═¼īW(xu©”)éāüĒųv┤_ėąŪ¦Ņ^╚fŠw���Īó┴”▓╗Å─ą─ų«Ėą����Ī�����Ż╗∙ė┌┤╦Ż¼╣Pš▀ĮY(ji©”)║ŽĮ╠īW(xu©”)īŹ(sh©¬)█`£\šäę╗Ž┬ėąĻP(gu©Īn)╦ßēA¹}Ą─Å═(f©┤)┴Ģ(x©¬)����Ż¼ęįŲ┌ī”═¼īW(xu©”)éāĄ─Å═(f©┤)┴Ģ(x©¬)ėą╦∙ų·ęµ�ĪŻ
ę╗Īó╩ņŠÜėøæøęÄ(gu©®)┬╔╩Ūæ¬(y©®ng)ė├Ą─Ū░╠ß
╦ßēA¹}▓┐Ęųļm╚╗Ņ}ą═▒ŖČÓ����Ż¼╚ńŻ║ĶbäeĪó═ŲöÓ�Īó│²ļs……Ż¼Ą½╩Ū▀@ą®æ¬(y©®ng)ė├ļx▓╗ķ_ūŅ╗∙ĄA(ch©│)Ą─ų¬ūR³c(di©Żn)Ż║╝┤Ż║ī”╦ßēA¹}╗»īW(xu©”)ąį┘|(zh©¼)Ą─╩ņŠÜėøæø����ĪŻ
═©▀^īW(xu©”)┴Ģ(x©¬)┐╔ų¬Ż║╦ߥ─═©ąįėą╬Õ³c(di©Żn)ĪóēA║═¹}Ą─═©ąįĖ„ėą╦─³c(di©Żn)�����ĪŻī”ė┌▀@ą®╗»īW(xu©”)ąį┘|(zh©¼)▒žĒÜ╝ėęįÅŖ(qi©óng)╗»ėøæø║═ņ`╗Ņėøæø�ĪŻ┐╔▓╔ė├łD▒ĒėøæøĘ©ęį╝░ūā╩ĮėøæøĘ©Ą╚��ĪŻ
╚ńŻ║īó╦ßēA¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)ØŌ┐s×ķŽ┬łDėøæø▌^║├(łD▒ĒėøæøĘ©)
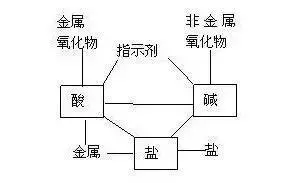
į┌┤╦╗∙ĄA(ch©│)╔ŽŻ¼į┘ū÷ūā╩ĮŠÜ┴Ģ(x©¬)��Ż¼į÷╝ėī”╗»īW(xu©”)ąį┘|(zh©¼)Ą─ČÓĮŪČ╚ėøæø(ūā╩ĮėøæøĘ©)��ĪŻ╚ńŻ║
(1)╔·│╔¹}║═╦«Ą─ęÄ(gu©®)┬╔���Ż¼ę╗Č©╩Ūųą║═Ę┤æ¬(y©®ng)åß?
(2)į┌╦ßēA¹}Ą─╗»īW(xu©”)ąį┘|(zh©¼)ųą���Ż¼╔·│╔¹}Ą─ęÄ(gu©®)┬╔ėąÄūŚlĄ╚ĪŻ
═©▀^╚ń╔ŽŠÜ┴Ģ(x©¬)�Ż¼╝┤┐╔ŲĄĮ╝ėÅŖ(qi©óng)ų¬ūRĄ─═¼╗»║═«É╗»Ą─ū„ė├ĪŻ
Č■�����ĪóšŲ╬š“ęÄ(gu©®)Šž”�����Ż¼┐╔│╔“ĘĮłA”
ėøæøūĪęį╔ŽęÄ(gu©®)┬╔Š═┐╔ęį╩ņŠÜæ¬(y©®ng)ė├┴╦åß?«ö(d©Īng)╚╗▓╗─▄���ĪŻį┌┤¾┴┐ŠÜ┴Ģ(x©¬)ųą═¼īW(xu©”)éā░l(f©Ī)¼F(xi©żn)ęį╔ŽęÄ(gu©®)┬╔ųąėą║▄ČÓ╩Ūėą “ęÄ(gu©®)Šž” ėąŚl╝■Ą─�����ĪŻę“┤╦į┌ėøūĪęÄ(gu©®)┬╔Ą─Ū░╠ߎ┬���Ż¼▀Ćę¬ėøūĪęÄ(gu©®)┬╔æ¬(y©®ng)ė├Ą─Śl╝■���Ż¼▀@śė▓┼─▄ū÷ĄĮėąĄ─Ę┼╩ĖĄ─æ¬(y©®ng)ė├ĪŻ▒╚╚ńŻ║┐╔Ė∙ō■(j©┤)▓╗═¼Ę┤æ¬(y©®ng)ŅÉą═üĒņ`╗ŅėøæøėąĻP(gu©Īn)Ę┤æ¬(y©®ng)Ą─Śl╝■�ĪŻÜw╝{╚ńŽ┬Ż║
└²╚ńŻ║īæ│÷Ž┬┴ą╬’┘|(zh©¼)ųąā╔ā╔ų«ķg─▄░l(f©Ī)╔·Ę┤æ¬(y©®ng)Ą─╗»īW(xu©”)ĘĮ│╠╩Į���ĪŻ
ĶF����Īóč§╗»ĶF�����Īó¤²ēA╚▄ę║�����ĪóŽĪ┴“╦ß����Īó┴“╦ßŃ~╚▄ę║�����Īó┬╚╗»õ^╚▄ę║��ĪóČ■č§╗»╠╝
╦╝┬Ę³c(di©Żn)ō▄Ż║
┤╦ŅÉŅ}─┐╩Ū┐╝▓ņ╦ß���ĪóēAĪó¹}����Īóč§╗»╬’ų«ķgĘ┤æ¬(y©®ng)ęÄ(gu©®)┬╔║═Ę┤æ¬(y©®ng)░l(f©Ī)╔·Śl╝■Ą─▌^║├ĘČ└²ĪŻĮŌŅ}Ģr���Ż¼×ķĘ└ų╣«a(ch©Żn)╔·üG┬õ¼F(xi©żn)Ž¾�Ż¼┐╔▓╔ė├ęįĶF×ķŲ³c(di©Żn)ų┤╬Ž“║¾čė╔ņ┼ąöÓĘ┤æ¬(y©®ng)╩Ūʱ░l(f©Ī)╔·�����Ż¼į┘ęįč§╗»ĶF×ķą┬Ų³c(di©Żn)ų┤╬Ēś═Ų……Ą─ĘĮĘ©�ĪŻĮø(j©®ng)┼ąöÓ╣▓░l(f©Ī)╔·8éĆĘ┤æ¬(y©®ng)ĪŻė╔ęį╔Ž┐╔ęį┐┤│÷Ż║į┌┼ąöÓĄ─▀^│╠ųą��Ż¼ūį╚╗ÅŖ(qi©óng)╗»┴╦ėąĻP(gu©Īn)Ę┤æ¬(y©®ng)ęÄ(gu©®)┬╔ęį╝░Ę┤æ¬(y©®ng)░l(f©Ī)╔·Śl╝■Ą─ėøæø��ĪŻ▀@śėĄ─┴Ģ(x©¬)Ņ}═¼īW(xu©”)éā┐╔ČÓšęę╗ą®Ż¼ū÷│╔┐©Ų¼│Żéõū¾ėę�����Ż¼ļSĢr╝ėęįŠÜ┴Ģ(x©¬)�����Ż¼╣”ĄĮūį╚╗│╔�����ĪŻ
╚²��Īóūźųž³c(di©Żn)Ņ}ą═��Ż¼īW(xu©”)Ģ■ęį³c(di©Żn)Ħ├µ
į┌Å═(f©┤)┴Ģ(x©¬)ųąĮø(j©®ng)│ŻęŖĄĮ▓╗╔┘═¼īW(xu©”)┬±Ņ^ė┌Ņ}║Żų«ųą�Ż¼║─ĢrķL╩šą¦╔§╬ó��ĪŻ╦ßēA¹}▓┐ĘųĄ─Ņ}ą═ļmą╬╩ĮČÓśė�����Ż¼Ą½╚fūā▓╗ļxŲõū┌�ĪŻŠC║Žų«Ž┬�����Ż¼┐╔ęįšfĶbäe�����Īó│²ļs�����Īó═ŲöÓ▀@╚²ŅÉŅ}ą═╩Ū║▄Š▀┤·▒ĒąįĄ─��Ż¼╦³éāĄ─š²┤_└ĒĮŌ║═šŲ╬š����Ż¼ī”ė┌╠ßĖ▀Ųõ╦¹ŽÓĻP(gu©Īn)Ņ}ą═Ą─æ¬(y©®ng)ūā─▄┴”�����Ż¼▒žīóŲĄĮ║▄║├Ą─▌Ś╔õū„ė├�ĪŻŽ┬├µĮY(ji©”)║ŽŽÓĻP(gu©Īn)└²Ņ}║åę¬?d©▓)w╝{ę╗Ž┬Ė„ūį╠ž³c(di©Żn)ĪŻ
└²ę╗Ż║Ęųäe▀xė├ę╗ĘNįćä®ĶbäeęįŽ┬Ė„ĮM╚▄ę║Ż║
A NaOH�ĪóNaCl╚▄ę║ĪóŽĪHCl ()
B Na2CO3ĪóAgNO3╚▄ę║����ĪóKNO3╚▄ę║ ()
C K2CO3ĪóBaCl2╚▄ę║����ĪóNaCl╚▄ę║ ( )
D NaOHĪóCa(OH)2╚▄ę║���ĪóŽĪHCl ( )
E NH4NO3����Īó(NH4)2SO4���ĪóNa2CO3ĪóNaCl╚▄ę║ ( )
╦╝┬Ę³c(di©Żn)ō▄Ż║
ĶbäeŅ}Ą─įŁät╩ŪŻ║ūźūĪ▓╗═¼╬’┘|(zh©¼)Ą─ų„ę¬╠žš„��Ż¼ė├ūŅ║åå╬Ą─ĘĮĘ©��Ż¼ūŅ╔┘Ą─įćä®��Ż¼ęįūŅ├„’@Ą─¼F(xi©żn)Ž¾�����Ż¼▀_(d©ó)ĄĮĶbäeĄ──┐Ą─ĪŻ╦∙ų^ūŅ║åå╬Ą─ĘĮĘ©╩ŪųĖ─▄ė├╬’└ĒĘĮĘ©ĶbäeĄ─Š═▓╗ę¬ė├╗»īW(xu©”)ĘĮĘ©Ķbäe;─▄ę╗┤╬ĶbäeĄ─Š═▓╗ė├ČÓ┤╬Ķbäe���ĪŻ╦∙ų^ūŅ╔┘įćä®���Ż¼Š═╩Ū─▄ė├ę╗ĘNįćä®Ķbäeķ_üĒĄ─Š═▓╗ę¬ė├ČÓĘNįćä®ĪŻ╦∙ų^ūŅ├„’@Ą─¼F(xi©żn)Ž¾�����Ż¼Š═╩Ū═©▀^īŹ(sh©¬)“×(y©żn)╩╣Ė„Ķbäe╬’┘|(zh©¼)ėą├„’@▓╗═¼Ą─¼F(xi©żn)Ž¾��ĪŻ╚ńŻ║«a(ch©Żn)╔·ūā╔½���ĪóĘ┼│÷ÜŌ¾w��Īó╔·│╔│┴ĄĒĄ╚��ĪŻ
ĮŌ╬÷Ż║A�����Īó═©▀^╬’┘|(zh©¼)ĘųŅÉ�����Ż¼’@╚╗ę└┤╬Ę¹║ŽēAąį��Īóųąąį����Īó╦ßąįŻ¼«ö(d©Īng)╚╗╝ė╩»╚’įćę║Ķbäe�ĪŻ
BĪó ═©▀^ė^▓ņ░l(f©Ī)¼F(xi©żn)Ż║Na2CO3ė÷╦ß(H+)«a(ch©Żn)╔·ÜŌ¾w�Ż¼Č°AgNO3ė÷CL-«a(ch©Żn)╔·│┴ĄĒŻ¼Č°KNO3ė÷¹}╦ߤo¼F(xi©żn)Ž¾��Ż¼╣╩╝ė¹}╦ßüĒĶbäe�����ĪŻ
C�Īóė╔╔Ž┐╔ų¬Ż║K2CO3ė÷╦ß(H+)«a(ch©Żn)╔·ÜŌ¾wŻ¼BaCl2╚▄ę║ė÷SO42-ėą│┴ĄĒ��Ż¼Č°NaCl╚▄ę║ė÷ŽĪ┴“╦ߤo¼F(xi©żn)Ž¾��Ż¼╣╩╝ėŽĪ┴“╦ßüĒĶbäe���ĪŻ
D�����ĪóCa(OH)2╚▄ę║ė÷CO32-ėą│┴ĄĒ�Ż¼ŽĪHCl ė÷CO32-ėąÜŌ¾w���Ż¼Č°NaOH ė÷CO32-¤o├„’@¼F(xi©żn)Ž¾�Ż¼╣╩╝ėNa2CO3╗“K2CO3Ķbäe�����ĪŻ
E����Īóė^▓ņ┐╔ų¬Ż║NH4+ė÷OH-«a(ch©Żn)╔·░▒ÜŌŻ¼Č°Ba2+ė÷CO32-��ĪóSO42-Š∙ėą│┴ĄĒ«a(ch©Żn)╔·�Ż¼╚Īśė║¾ĘųäeĄ╬╝ėBa(OH)2╚▄ę║Ż¼ų╗ėąÜŌ¾w«a(ch©Żn)╔·Ą─╩ŪNH4NO3��Ż¼═¼ĢrėąÜŌ¾w║═│┴ĄĒ«a(ch©Żn)╔·Ą─╩Ū(NH4)2SO4�Ż¼ų╗ėą│┴ĄĒ«a(ch©Żn)╔·Ą─╩ŪNa2CO3��Ż¼¤o¼F(xi©żn)Ž¾Ą─╩ŪNaCl�ĪŻ
į┌īŹ(sh©¬)ļHæ¬(y©®ng)ė├ųą�����Ż¼═¼īW(xu©”)éā▀Ć┐╔ęįīóĶbäeŅ}░┤ę╗┤╬ąįĶbäe���ĪóČÓ┤╬ąįĶbäe�Īó▓╗╝ėŲõ╦¹įćä®Ķbäe����Īóā╔ā╔╗ņ║ŽĶbäeĄ╚▀M(j©¼n)ąąĘųŅÉŻ¼Ė∙ō■(j©┤)Ė„ūį¬Ü(d©▓)ėąĄ─╠ž³c(di©Żn)����Ż¼┐éĮY(ji©”)ĮŌŅ}╝╝Ū╔Ż¼Å─Č°▀_(d©ó)ĄĮ╚½├µšŲ╬š▓╗═¼ĶbäeŅÉą═Ą──┐Ą─�����ĪŻ
└²Č■Ż║▀xė├║Ž▀mĄ─ĘĮĘ©│²╚źŽ┬┴ą╬’┘|(zh©¼)ųąĄ─╔┘┴┐ļs┘|(zh©¼)
(1)│²╚ź╔·╩»╗ęųąĄ─╠╝╦ßŌ}
(2)│²╚ź┬╚╗»ŌøŠ¦¾wųąĄ─╠╝╦ßŌø
(3)│²╚ź╠╝╦ßŌ}╣╠¾wųąĄ─╠╝╦ßŌc
(4)│²╚źę╗č§╗»╠╝ųąĄ─Č■č§╗»╠╝
(5)│²╚ź┬╚╗»Ōc╚▄ę║ųąĄ─┴“╦ßŃ~
(6)│²╚źCuĘ█ųąĄ─FeĘ█
╦╝┬Ę³c(di©Żn)ō▄Ż║
│²ļsĄ─įŁät╩ŪŻ║▓╗į÷(▓╗į÷╝ėą┬ļs┘|(zh©¼))���Īó▓╗£p(▓╗£p╔┘įŁ╬’┘|(zh©¼)Ą─┴┐)����Īó▓╗ūā(▓╗Ė─ūāįŁ╬’┘|(zh©¼)ĀŅæB(t©żi))���ĪóęūĘų(│²ļs║¾ęūė┌Ęųļx)��ĪóŽ╚╬’║¾╗»(╬’└ĒĘĮĘ©ā×(y©Łu)Ž╚��Ż¼Ųõ┤╬╗»īW(xu©”)ĘĮĘ©)�ĪŻæ¬(y©®ng)ė├ųąėą▐D(zhu©Żn)╗»Ę©���Īó│┴ĄĒĘ©�Īó╬³╩šĘ©����Īó▀^×VĘ©Īó╚▄ĮŌĘ©Ą╚ČÓĘN│²ļsĘĮĘ©����ĪŻ
ĮŌ╬÷Ż║(1)═©▀^Ė▀£ž╝ė¤ß╗“ūŲ¤²Ą─ĘĮĘ©Ż¼╝╚─▄│²╚ź╠╝╦ßŌ}����Ż¼ėų─▄Ą├ĄĮĖ³ČÓ╔·╩»╗ę��ĪŻ
(2)┐╔╝ė╚ļ▀m┴┐ŽĪ¹}╦ß│õĘųĘ┤æ¬(y©®ng)║¾�Ż¼į┘š¶░l(f©Ī)�ĪŻ
(3)┐╔▓╔ė├Ž╚╝ė▀m┴┐╦«╚▄ĮŌŻ¼į┘▀^×VĄ─ĘĮĘ©��ĪŻ
(4)┐╔▓╔ė├═©▀^¤ļ¤ßĄ─╠╝īė╗“═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©���ĪŻĄ½’@╚╗═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©Š▀ėą╬³╩šļs┘|(zh©¼)ÅžĄū�Īó▓┘ū„║åå╬┐ņĮ▌Ą╚ā×(y©Łu)³c(di©Żn)�����ĪŻ
(5)ė╔ė┌║¼ėąCu2+����ĪóSO42-ā╔ĘNļs┘|(zh©¼)ļxūėŻ¼╣╩┐╔▓╔ė├═¼Ģr│┴ĄĒĘ©��ĪŻ╝ė╚ļ▀m┴┐Üõč§╗»õ^╚▄ę║║¾�Ż¼▀^×V╝┤┐╔Ą├┬╚╗»Ōc╚▄ę║ĪŻ
(6)ė╔ė┌Fe�����ĪóCuĘųäe┼┼į┌Įī┘╗ŅäėĒśą“▒ĒųąHĄ─Ū░║¾Ż¼╦∙ęį┐╔▓╔ė├╝ė╚ļūŃ┴┐ŽĪ¹}╦ß╗“ŽĪ┴“╦ß╚▄ĮŌ▓ó▀^×VĄ─ĘĮĘ©üĒīŹ(sh©¬)¼F(xi©żn)��ĪŻę▓┐╔▓╔ė├╝ėūŃ┴┐┴“╦ßŃ~╚▄ę║▓ó▀^×VĄ─ĘĮĘ©����ĪŻ
└²╚²���Īóėąę╗╣╠¾w╗ņ║Ž╬’���Ż¼┐╔─▄║¼ėąK2CO3ĪóK2SO4�ĪóCuSO4ĪóCaCl2��ĪóKNO3Ą╚╬’┘|(zh©¼)ųąĄ─ę╗ĘN╗“ÄūĘN�����Ż¼īó╗ņ║Ž╬’╚▄ė┌╦«����Ż¼Ą├¤o╔½╚▄ę║Ż¼«ö(d©Īng)?sh©┤)╬╚ļŽ§╦ßõ^╚▄ę║Ģr����Ż¼ėą░ū╔½│┴ĄĒ«a(ch©Żn)╔·���Ż¼į┘╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌŻ¼ätįō╗ņ║Ž╬’ųąę╗Č©║¼ėą_____ę╗Č©▓╗║¼ėą_____┐╔─▄║¼ėą____.
╦╝┬Ę³c(di©Żn)ō▄Ż║
═ŲöÓŅ}╦∙ė├ĄĮĄ─ų¬ūRā”éõėą╚ńŽ┬Äū³c(di©Żn)Ż║
(1)╬’┘|(zh©¼)Ą─╠ž╩Ō╔½æB(t©żi)�����Īó╚▄ĮŌąį(░³└©╬’┘|(zh©¼)į┌╦«╗“╦ßųąĄ─╚▄ĮŌąį)�ĪŻ╚ńŻ║Ń~ļxūė╚▄ę║×ķ╦{(l©ón)╔½Ż¼ĶFļxūė╚▄ę║×ķ³S╔½Ą╚���Ż¼│ŻęŖ░ū╔½│┴ĄĒėą╠╝╦ßŌ}����Īó╠╝╦ßõ^���Īó╠╝╦ßŃy�Īó┬╚╗»Ńy����Īó┴“╦ßõ^ĪóÜõč§╗»µVĄ╚ĪŻ╦{(l©ón)╔½│┴ĄĒėąÜõč§╗»Ń~�����Ż¼╝t║ų╔½│┴ĄĒėąÜõč§╗»ĶF��ĪŻ│§ųą▓╗╚▄ė┌╦ߥ─│┴ĄĒėą┬╚╗»Ńy�Īó┴“╦ßõ^ĪŻ
(2)Ģ■┼ąöÓ╬’┘|(zh©¼)ų«ķg─▄ʱ░l(f©Ī)╔·Ę┤æ¬(y©®ng)���ĪŻ
(3)╚²ĘNļxūė(┴“╦ßĖ∙Īó╠╝╦ßĖ∙����Īó┬╚ļxūė)ĶbČ©Ą─š²─µ═Ų└ĒĪŻ
(4)ī”ė┌ųž³c(di©Żn)į~šZĄ─└ĒĮŌ─▄┴”����ĪŻ╚ńŻ║“╚½▓┐╚▄”Īó“▓┐Ęų╚▄”���Īó“╚½▓╗╚▄”Ą╚į~Ą─└ĒĮŌ����ĪŻę╗Ą└║├Ą─═ŲöÓŅ}š²╩Ūī”ė┌ęį╔Žų¬ūR³c(di©Żn)šŲ╬š│╠Č╚Ą─ŠC║Žąį┐╝▓ņĪŻ
ĮŌ╬÷Ż║═ŲöÓŅ}Ą─ĮŌ┤ę└ō■(j©┤)╩Ū╬’┘|(zh©¼)Ą─╠žš„Ę┤æ¬(y©®ng)║═Ąõą═Ą─īŹ(sh©¬)“×(y©żn)¼F(xi©żn)Ž¾��ĪŻ┤╦Ņ}ė╔╚▄ė┌╦«Ą├ĄĮ“¤o╔½╚▄ę║”┐╔ų¬Ż║CuSO4(╦{(l©ón)╔½╚▄ę║)ę╗Č©▓╗┤µį┌;═¼ĢrK2CO3�ĪóCaCl2ė╔ė┌ŽÓė÷Ģ■«a(ch©Żn)╔·│┴ĄĒŻ¼╦∙ęįK2CO3��ĪóCaCl2╗“┤µŲõę╗╗“Š∙▓╗┤µį┌����ĪŻė╔“Ą╬╝ėŽ§╦ßõ^╚▄ę║ĢrŻ¼ėą░ū╔½│┴ĄĒ«a(ch©Żn)╔·”┐╔ų¬Ż║│┴ĄĒėą┐╔─▄üĒūįŽ§╦ßõ^┼cK2CO3╗“K2SO4Ę┤æ¬(y©®ng)╔·│╔Ą─╠╝╦ßõ^���Īó┴“╦ßõ^│┴ĄĒųąĄ─ę╗š▀╗“ā╔š▀�ĪŻė╔“╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌ”┐╔ų¬Ż║╠╝╦ßõ^���Īó┴“╦ßõ^Š∙┤µį┌�����Ż¼▀M(j©¼n)Č°═Ų│÷K2CO3�ĪóK2SO4Š∙┤µį┌����ĪŻę“?y©żn)ķK2CO3┤µį┌��Ż¼╦∙ęįCaCl2ę╗Č©▓╗┤µį┌��ĪŻČ°KNO3ė╔ė┌┤µį┌┼cʱ�Ż¼Š∙▓╗Ģ■ī”ęį╔ŽĶbäe═ŲöÓįņ│╔ė░Ēæ����Ż¼╦∙ęįKNO3┐╔─▄┤µį┌Ż¼ę▓┐╔ęįšf┐╔─▄▓╗┤µį┌�����ĪŻ
┤╦Ņ}�����Ż¼į┌ŠÜ┴Ģ(x©¬)▀^│╠ųą�Ż¼═Ļ╚½┐╔ęį┬į╝ėĖ─äė�����ĪŻ╚ńŻ║╚¶“│┴ĄĒ╚½▓┐╚▄ĮŌ”═ŲöÓĮY(ji©”)╣¹į§śė?╚¶“│┴ĄĒ╚½▓╗╚▄”═ŲöÓĮY(ji©”)╣¹ėųĢ■į§śė?……�ĪŻ═¼īW(xu©”)éāę╗Ą®šŲ╬š┴╦▀@ĘNę╗Ņ}ČÓūāĪóę╗Ņ}ČÓū÷Ą─īW(xu©”)┴Ģ(x©¬)ĘĮĘ©����Ż¼ī”ė┌╠ßĖ▀Å═(f©┤)┴Ģ(x©¬)ą¦╣¹▒ž╚╗┐╔ęįŲĄĮęį³c(di©Żn)Ħ├µĄ─▌Ś╔õū„ė├���ĪŻ
│§╚²╗»īW(xu©”)Ż║ėąĻP(gu©Īn)╦ßēA¹}Ą─╗»īW(xu©”)ĘĮ│╠╩Į
å╬┘|(zh©¼)Īóč§╗»╬’���Īó╦ß�ĪóēA���Īó¹}Ą─ŽÓ╗źĻP(gu©Īn)ŽĄ
(1)Įī┘å╬┘|(zh©¼) + ╦ß --- ¹} + ÜõÜŌ (ų├ōQĘ┤æ¬(y©®ng))
1. õ\║═ŽĪ┴“╦ßZn + H2SO4 = ZnSO4 + H2↑ (ūŅ│Żė├)
(īŹ(sh©¬)“×(y©żn)╩ęųŲH2ė├Ą─Įī┘ėąZn,Fe,Mg,Al����Ż¼╦ßėąŽĪH2SO4║═ŽĪHCl )
(2)Įī┘å╬┘|(zh©¼) + ¹}(╚▄ę║) --- ┴Ēę╗ĘNĮī┘ + ┴Ēę╗ĘN¹}
2. ĶF║═┴“╦ßŃ~╚▄ę║Ę┤æ¬(y©®ng)Ż║Fe + CuSO4 = FeSO4 +
3. õX║═Ž§╦ßŃy╚▄ę║Ę┤æ¬(y©®ng)Ż║Al+ 3AgNO3 = Al(NO3)3 + 3Ag
(3)ēAąįč§╗»╬’(Įī┘č§╗»╬’) +╦ß --- ¹} + ╦«
4. č§╗»ĶF║═ŽĪ┴“╦ßĘ┤æ¬(y©®ng)Ż║Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
5. č§╗»Ō}║═ŽĪ¹}╦ßĘ┤æ¬(y©®ng)Ż║CaO + 2HCl = CaCl2 + H2O
(4)╦ßąįč§╗»╬’(ĘŪĮī┘č§╗»╬’) +ēA -------- ¹} + ╦«
6.┐┴ąįŌc▒®┬Čį┌┐šÜŌųąūā┘|(zh©¼)Ż║2NaOH + CO2 = Na2CO3 + H2O
7.Ž¹╩»╗ęĘ┼į┌┐šÜŌųąūā┘|(zh©¼)Ż║Ca(OH)2 + CO2 = CaCO3 ↓+ H2O
(5)╦ß + ēA -------- ¹} + ╦« (ųą║═Ę┤æ¬(y©®ng))
8.¹}╦ß║═¤²ēAĘ┤æ¬(y©®ng)Ż║HCl + NaOH = NaCl +H2O
9. ¹}╦ß║═Üõč§╗»Ō}Ę┤æ¬(y©®ng)Ż║2HCl + Ca(OH)2 = CaCl2 + 2H2O
10.Üõč§
(6)╦ß + ¹} -------- ┴Ēę╗ĘN╦ß + ┴Ēę╗ĘN¹}
11.┤¾└Ē╩»┼cŽĪ¹}╦ßĘ┤æ¬(y©®ng)Ż║CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ (īŹ(sh©¬)“×(y©żn)╩ęųŲCO2)
12.╠╝╦ßŌc┼cŽĪ¹}╦ßĘ┤æ¬(y©®ng): Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
13.┴“╦ß║═┬╚╗»õ^╚▄ę║Ę┤æ¬(y©®ng)Ż║H2SO4 + BaCl2 = BaSO4 ↓+ 2HCl
(7)ēA + ¹} --- ┴Ēę╗ĘNēA + ┴Ēę╗ĘN¹}
14. Üõč§╗»Ō}┼c╠╝╦ßŌcŻ║Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH
15.┴“╦ßŃ~╚▄ę║┼cÜõč§╗»õ^Ż║
CuSO4 + Ba(OH)2 = BaSO4↓+ Cu(OH)2↓
(8)¹} + ¹} --- ā╔ĘNą┬¹}
16.┬╚╗»Ōc╚▄ę║║═Ž§╦ßŃy╚▄ę║Ż║NaCl + AgNO3 = AgCl↓ + NaNO
17.┴“╦ßŌc║═┬╚╗»õ^Ż║Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
Å═(f©┤)ĘųĮŌĘ┤æ¬(y©®ng)▒žĒÜ╔·│╔│┴ĄĒ�����Ż¼ÜŌ¾w╗“╦«╔·│╔▓┼─▄░l(f©Ī)╔·�����Ż¼Ūę╔·│╔╬’Ą─į¬╦ž╗»║Žār▓╗ūā���ĪŻ
+1ār:HClO ;NaClO;Ca(ClO)2.
+5ār:HClO3 ;KClO3.
+7ār:HClO4 ;KClO4.
╗»īW(xu©”)╦ßēA¹}▌oī¦(d©Żo)Ż║╣¹ŽÓ═¼����Ż¼ę“ėą«É
│§ųą╗»īW(xu©”)Ą┌░╦š┬ųąŻ¼┤µį┌ų°ę╗ą®ĮY(ji©”)╣¹(ĮY(ji©”)šō)ŽÓ═¼����ĪóįŁę“ėą«ÉĄ─å¢Ņ}Ż¼¼F(xi©żn)ć·└@╦ß�ĪóēAĄ─ėąĻP(gu©Īn)ų¬ūRŻ¼▀x╚ĪÄū└²╝ėęįĘų╬÷���ĪŻ
1.╦ß�����ĪóēA╚▄ę║║═Įī┘Č╝─▄ī¦(d©Żo)ļŖ���ĪŻ
Ęų╬÷Ż║╦ß���ĪóēA╚▄ę║ī¦(d©Żo)ļŖĄ─įŁę“╩Ū���Ż¼╦ßĪóēA╚▄ę║ųą║¼ėąūįė╔ęŲäėĄ─ļxūė(Ųõųą╦ß╚▄ę║ųą║¼ėąūįė╔ęŲäėĄ─Üõļxūė║═╦ßĖ∙ļxūė;ēA╚▄ę║ųą║¼ėąūįė╔ęŲäėĄ─Įī┘ļxūė║═Üõč§Ė∙ļxūė);Įī┘ī¦(d©Żo)ļŖĄ─įŁę“╩Ū�����Ż¼Įī┘ųą║¼ėąūįė╔ęŲäėĄ─ļŖūėĪŻ
2.ØŌ¹}╦ß��ĪóØŌ¹}╦ß│©┐┌ų├ė┌┐šÜŌųą����Ż¼╚▄ę║ųą╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)Č╝ūāąĪĪŻ
Ęų╬÷Ż║ØŌ┴“╦ßųą╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)ų«╦∙ęįūāąĪ��Ż¼╩Ūę“?y©żn)ķØŌ┴“╦ߊ▀ėą╬³╦«ąį�����Ż¼ØŌ┴“╦ß╬³╩š┐šÜŌųąĄ─╦«Ęųī?d©Żo)ų┬┴╦╚▄ę║ųą╚▄ä®┴┐Ą─į÷╝ė;ØŌ¹}╦ßųą╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ęų?j©½n)?sh©┤)ų«╦∙ęįūāąĪ���Ż¼╩Ūę“?y©żn)ķØŌ¹}╦ߊ▀ėąō]░l(f©Ī)ąį����Ż¼┬╚╗»ÜõÜŌ¾wĄ─ō]░l(f©Ī)ī¦(d©Żo)ų┬┴╦╚▄ę║ųą╚▄┘|(zh©¼)┘|(zh©¼)┴┐Ą─£p╔┘���ĪŻ
3.ØŌ┴“╦ß�����ĪóÜõč§╗»Ōc╚▄ė┌╦«����Ż¼╔·╩»╗ęĘ┼╚ļ╦«ųąŻ¼Č╝─▄Ę┼│÷┤¾┴┐Ą─¤ß��ĪŻ
Ęų╬÷Ż║ØŌ┴“╦ß����ĪóÜõč§╗»Ōc╚▄ė┌╦«Ę┼¤ßŻ¼ī┘ė┌╚▄ĮŌ▀^│╠ųąĄ─Ę┼¤ß¼F(xi©żn)Ž¾;╔·╩»╗ę┼c╦«Įėė|Ę┼¤ß����Ż¼ī┘ė┌╗»īW(xu©”)ūā╗»(╔·╩»╗ę┼c╦«░l(f©Ī)╔·╗»īW(xu©”)Ę┤æ¬(y©®ng)Ż¼╔·│╔Üõč§╗»Ō})ųąĄ─Ę┼¤ß¼F(xi©żn)Ž¾��ĪŻ
4.Įī┘Ōc║═µVĘ┼╚ļŽĪ¹}╦ßųą����Ż¼Č╝ėąÜõÜŌĘ┼│÷ĪŻ
Ęų╬÷Ż║Įī┘ŌcĘ┼╚ļŽĪ¹}╦ßųą╦∙Ę┼│÷Ą─ÜõÜŌ�Ż¼ų„ę¬╩Ūė╔Ōc┼c╦«░l(f©Ī)╔·ų├ōQĘ┤æ¬(y©®ng)«a(ch©Żn)╔·Ą─(į┌Įī┘╗ŅäėĒśą“▒Ēųą├¹┴ąĄ┌╚²Ą─Įī┘Ōc�Ż¼Ųõ╗»īW(xu©”)ąį┘|(zh©¼)ĘŪ│Ż╗ŅØŖ���Ż¼─▄į┌│Ż£žŽ┬┼c╦«░l(f©Ī)╔·äĪ┴ęĘ┤æ¬(y©®ng)Ż║
2Na+2H2O==2NaOH+H2↑);µVĘ┼╚ļŽĪ¹}╦ßųą╦∙«a(ch©Żn)╔·Ą─ÜõÜŌ��Ż¼╩ŪµV║═ŽĪ¹}╦ß░l(f©Ī)╔·ų├ōQĘ┤æ¬(y©®ng)«a(ch©Żn)╔·Ą─��ĪŻ
5.Üõč§╗»Ōc╚▄ę║┼c┴“╦ßŃ~╚▄ę║���ĪóŽĪ¹}╦ß┼c╠╝╦ßŌc╚▄ę║░l(f©Ī)╔·Ę┤æ¬(y©®ng)(╝┘įO(sh©©)ā╔éĆĘ┤æ¬(y©®ng)Č╝ŪĪ║├═Ļ╚½░l(f©Ī)╔·)║¾�����Ż¼╚▄ę║Ą─┐é┘|(zh©¼)┴┐Č╝£p╔┘��ĪŻ
Ęų╬÷Ż║Ė∙ō■(j©┤)╔Ž╩÷ūā╗»Ą─╗»īW(xu©”)ĘĮ│╠╩Įęį╝░┘|(zh©¼)┴┐╩ž║ŃČ©┬╔┐╔ęįĄ├│÷�Ż¼Ū░ę╗éĆĘ┤æ¬(y©®ng)║¾╦∙Ą├╚▄ę║Ą─┘|(zh©¼)┴┐==Üõč§╗»Ōc╚▄ę║Ą─┘|(zh©¼)┴┐+┴“╦ßŃ~╚▄ę║Ą─┘|(zh©¼)┴┐-╔·│╔Ą─Üõč§╗»Ń~│┴ĄĒĄ─┘|(zh©¼)┴┐;║¾ę╗éĆĘ┤æ¬(y©®ng)║¾╦∙Ą├╚▄ę║Ą─┘|(zh©¼)┴┐==ŽĪ¹}╦ߥ─┘|(zh©¼)┴┐+╠╝╦ßŌc╚▄ę║Ą─┘|(zh©¼)┴┐-Ę┼│÷Ą─Č■č§╗»╠╝Ą─┘|(zh©¼)┴┐�����ĪŻļm╚╗ā╔éĆĘ┤æ¬(y©®ng)ųą╚▄ę║Ą─┐é┘|(zh©¼)┴┐Č╝£p╔┘�Ż¼Ą½įŁę“▓╗═¼Ż¼ę╗éĆ╩Ūę“?y©żn)ķĘ┤æ?y©®ng)ųą«a(ch©Żn)╔·│┴ĄĒ�Ż¼ę╗éĆ╩Ūę“?y©żn)ķĘ┤æ?y©®ng)ųąĘ┼│÷ÜŌ¾wĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖC(j©®)����ĪóŲĮ░ÕĄ╚ęŲäėįO(sh©©)éõįLå¢ųą┐╝ŠW(w©Żng)����Ż¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąą��ŻĪ>>³c(di©Żn)ō¶▓ķ┐┤















