常見的酸
1.生活中常用的酸:胃液中含有的鹽酸(HCl)�,蓄電池中含有硫酸(H2SO4)����,酸雨中含有的硫酸及硝酸(HNO3)�����,食醋中含有的醋酸(CH3COOH或HAc);飲料中可能含有的碳酸����、檸檬酸等。
2.酸的分類:無氧酸(如HCl)�、含氧酸(HNO3、H2SO4)等����。
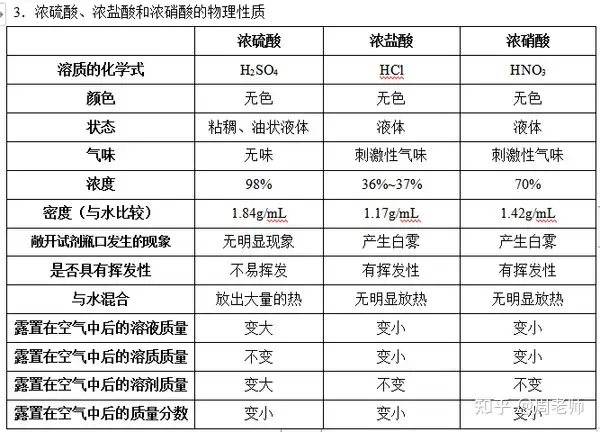
注意:濃硫酸具有一定的特性:
(1)吸水性(物理性質(zhì))用于氣體干燥,但除NH3等堿性氣體除外[2NH3+ H2SO4== (NH4)2SO4]
(2)脫水性(化學(xué)性質(zhì))——黑面包實(shí)驗(yàn)(濃硫酸與蔗糖反應(yīng)�,使之炭化。)
(3)強(qiáng)氧化性����,腐蝕性——與金屬發(fā)生反應(yīng),生成的氣體不生成氫氣而是二氧化硫。
在加熱的條件下��,能與排在氫后面的金屬(如Cu)反應(yīng)����,如:
Cu+2H2SO4(濃)△==CuSO4+SO2↑+H2O
又如,冷的濃硫酸與鐵或鋁反應(yīng)后���,能生成一層致密的氧化膜����,阻止反應(yīng)進(jìn)一步進(jìn)行�����。
(4)濃硫酸的稀釋:酸入水���,沿器壁�����,不斷攪拌���。
濃硫酸溶于水放出大量的水���,足以使水分沸騰,并且水的密度小于濃硫酸的密度��。如果把水倒入濃硫酸中��,水就會(huì)浮在濃硫酸上面�,溶解時(shí)放出大量的熱,致使水沸騰而使硫酸液滴向四周飛濺而造成事故���。
(5)安全事故的處理:濃硫酸濺到皮膚上后,首先迅速用抹布將其擦拭�����,然后用大量水沖洗����,最后用3%~5%的NaHCO3涂敷。
稀硫酸濺到皮膚上后�,應(yīng)該馬上沖洗,因?yàn)殡S著稀硫酸中溶劑的蒸發(fā)�����,也會(huì)變成濃硫酸。
4.酸的化學(xué)性質(zhì)
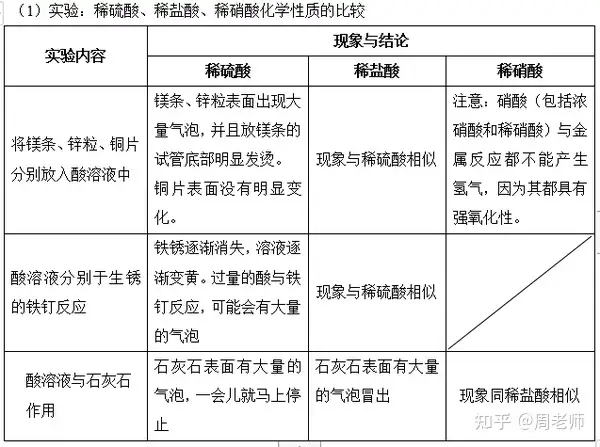
總結(jié):酸所具有的共同特點(diǎn):
酸在水溶液中都能電離出氫離子�����,因此酸溶液會(huì)具有許多共同的性質(zhì)(酸的五大通性):
(1)酸溶液與酸堿指示劑的反應(yīng)
A.紫色石蕊試液或藍(lán)色石蕊試紙遇到酸溶液變紅色;
B.無色酚酞試劑遇到酸溶液不變色���。
提醒:紫色石蕊試劑變色情況為:“酸紅堿藍(lán)”;是指示劑變色��,而非待測(cè)溶液本身變色���。
(2)酸溶液與某些金屬反應(yīng)
酸溶液+ (氫前)金屬→ 鹽溶液+ 氫氣
注意:
A.在金屬活動(dòng)性順序表中,排在氫前面的金屬能置換出酸中的氫�,排在氫后面的金屬則不能;
B.排在金屬活動(dòng)性順序表越前面的金屬,反應(yīng)現(xiàn)象越劇烈�����,速度越快��,如Mg反應(yīng)有明顯放
熱現(xiàn)象;
C.強(qiáng)氧化性酸與金屬反應(yīng)后��,不能生成氫氣�����,而是生成水。如濃硫酸�����、硝酸等強(qiáng)氧化性酸;
D.該類反應(yīng)屬于置換反應(yīng)
如:Zn + 2HCl == ZnCl2+ H2↑;Fe + H2SO4== FeSO4 + H2↑
(3)酸溶液與某些金屬氧化物反應(yīng)(金屬氧化物又稱堿性氧化物)
酸溶液+ 金屬氧化物→ 鹽溶液+ 水
注意:該反應(yīng)過程中����,金屬元素的化合價(jià)不變,酸中的原子團(tuán)不變
如:CuO + 2HCl == CuCl2+ H2O;Fe2O3+ 3H2SO4== Fe2(SO4)3+ 3H2O
ZnO + 2HNO3== Zn(NO3)2+H2O
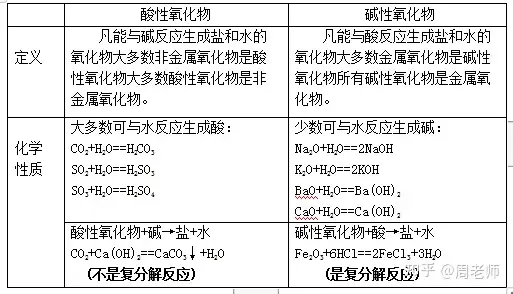
(4)酸溶液與堿的反應(yīng)(又稱為中和反應(yīng))
酸+堿→鹽+水
(5)酸溶液與某些鹽反應(yīng)
酸溶液+ 鹽→ 新酸+ 新鹽
注意:A.我們通常遇到的鹽是碳酸鹽��,因此絕大部分反應(yīng)是:
酸+ 碳酸鹽→ 新鹽+ 水+ 二氧化碳
如:CaCO3+ 2HCl == CaCl2+ H2O + CO2↑;Na2CO3+ H2SO4== Na2SO4+ H2O + CO2↑;
K2CO3+ 2HNO3== 2KNO3+ H2O + CO2↑;
MgCO3+ CH3COOH == (CH3COO)2Mg + H2O + CO2↑;
B.某些特殊的鹽能與酸反應(yīng)���,生成特殊的沉淀
如:HCl + AgNO3== AgCl↓+ HNO3;BaCl2+ H2SO4== BaSO4↓+ 2HCl
補(bǔ)充:Cl-及SO42-的檢驗(yàn)
A.向待測(cè)溶液中加入AgNO3溶液后有白色沉淀生成,滴入稀硝酸溶液后�����,沉淀不消失�,則溶液中含有Cl-,如果沒有沉淀或者沉淀消失���,則不含有Cl-���。
B.向待測(cè)溶液中加入Ba(NO3)2溶液后有白色沉淀生成���,滴入稀硝酸溶液后,沉淀不消失�����,則溶液中含有SO42-����,如果沒有沉淀或者沉淀消失,則不含有SO42-��。
歡迎使用手機(jī)����、平板等移動(dòng)設(shè)備訪問中考網(wǎng),2024中考一路陪伴同行�����!>>點(diǎn)擊查看












